Медиатека
Будущее в пробирке: ЭКО человека и животных
Оглавление:
•
История технологии ЭКО
•
Что такое ЭКО? Основные стадии
•
Немного статистики
1. Синдром гиперстимуляции яичников (СГЯ)
2. Многоплодная беременность или роды
3. Внематочная беременность
•
Эко животных
•
Проблемы и будущее ЭКО
2. Многоплодная беременность или роды
3. Внематочная беременность
Бесплодие давно является глобальной проблемой, затрагивающей миллионы людей во всем мире. Согласно Всемирной организацией здравоохранения, 15% пар репродуктивного возраста не могут зачать ребенка 1. Для борьбы с этой болезнью в 80-х годах прошлого столетия разработали терапию ЭКО, или экстракорпоральное оплодотворение человека – за это в 2010 году физиолог Роберт Эдвардс был удостоен Нобелевской премии 2. Его достижения вкупе с работами других ученых наконец сделали возможным лечение бесплодия. Сегодня ЭКО, недавно отпраздновавшее своё 40-летие, широко применяется как среди людей, так и среди животных 3.
История технологии ЭКО
Началом истории ЭКО можно считать 1959 г., когда ученый Мин Чуе Чанг, опираясь на более ранние работы, продемонстрировал процесс ЭКО у млекопитающих, оплодотворив ооциты кролика in vitro и получив жизнеспособные эмбрионы, а затем и здоровое потомство. На тот момент это стало окончательным доказательством возможности искусственного оплодотворения млекопитающих, вдохновив ученых по всему миру на продолжение экспериментов 4, 5.
Основателями же современного метода ЭКО человека заслуженно считаются Роберт Эдвардс и акушер-гинеколог Патрик Стептоу. Эдвардс начал исследования еще в 50-е годы, когда процесс ЭКО уже был продемонстрирован на кроликах. Он хотел выяснить, можно ли использовать подобные методы для оплодотворения яйцеклеток человека 2.
Многолетние эксперименты и исследования увенчались успехом к 1969 году, когда впервые удалось оплодотворить человеческую яйцеклетку в пробирке. Однако она делилась лишь один раз и дальнейшего развития не происходило. Эдвардс предположил, что необходимо взять яйцеклетку, созревшую в яичнике, но не знал, как достать такую клетку, не повредив при этом здоровью женщины-донора. Тогда он взял в партнеры Стептоу, одного из пионеров лапароскопии — метода, который позволял осматривать яичники с помощью оптического прибора. Стептоу использовал лапароскоп для удаления яйцеклеток из яичников — такие яйцеклетки после оплодотворения делились несколько раз и образовывали восьмиклеточные зародыши.
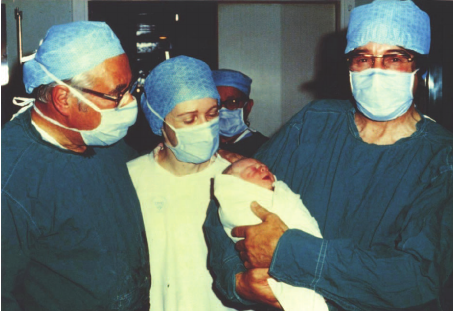
Несмотря на долгую историю научных и технологических инноваций, а также собственные успехи Эдвардса и его команды, прошло почти десятилетие после первого успешного оплодотворения человеческой яйцеклетки in vitro в 1969 году до рождения человека. Луиза Браун, первый в мире «ребенок из пробирки», родилась 25 июля 1978 года в больнице в Олдем, Великобритания 2.
Рис. 1. Патрик Стептоу, Джин Парди и Роберт Эдвардс на рождении Луизы Браун 25 июля 1978 года. Источник: Bourn Hall.
Так, 1978 год ознаменовался новой вехой в истории репродуктивной медицины. Успех Эдвардса Стептоу открыл двери для быстрого распространения технологии ЭКО по всему миру: в 1980 году в результате искусственного оплодотворения появился первый новорожденный в Австралии, в 1981 году — в США, а затем и в других странах. Искусственное оплодотворение, описанное в научно-фантастическом романе «О дивный новый мир» еще в 1932 году, наконец стало реальностью 5.
Что такое ЭКО? Основные стадии
ЭКО представляет собой имитацию естественных физиологических процессов, таких как развитие фолликулов, созревание ооцитов, оплодотворение и имплантацию, часть из которых проводится in vitro 6.
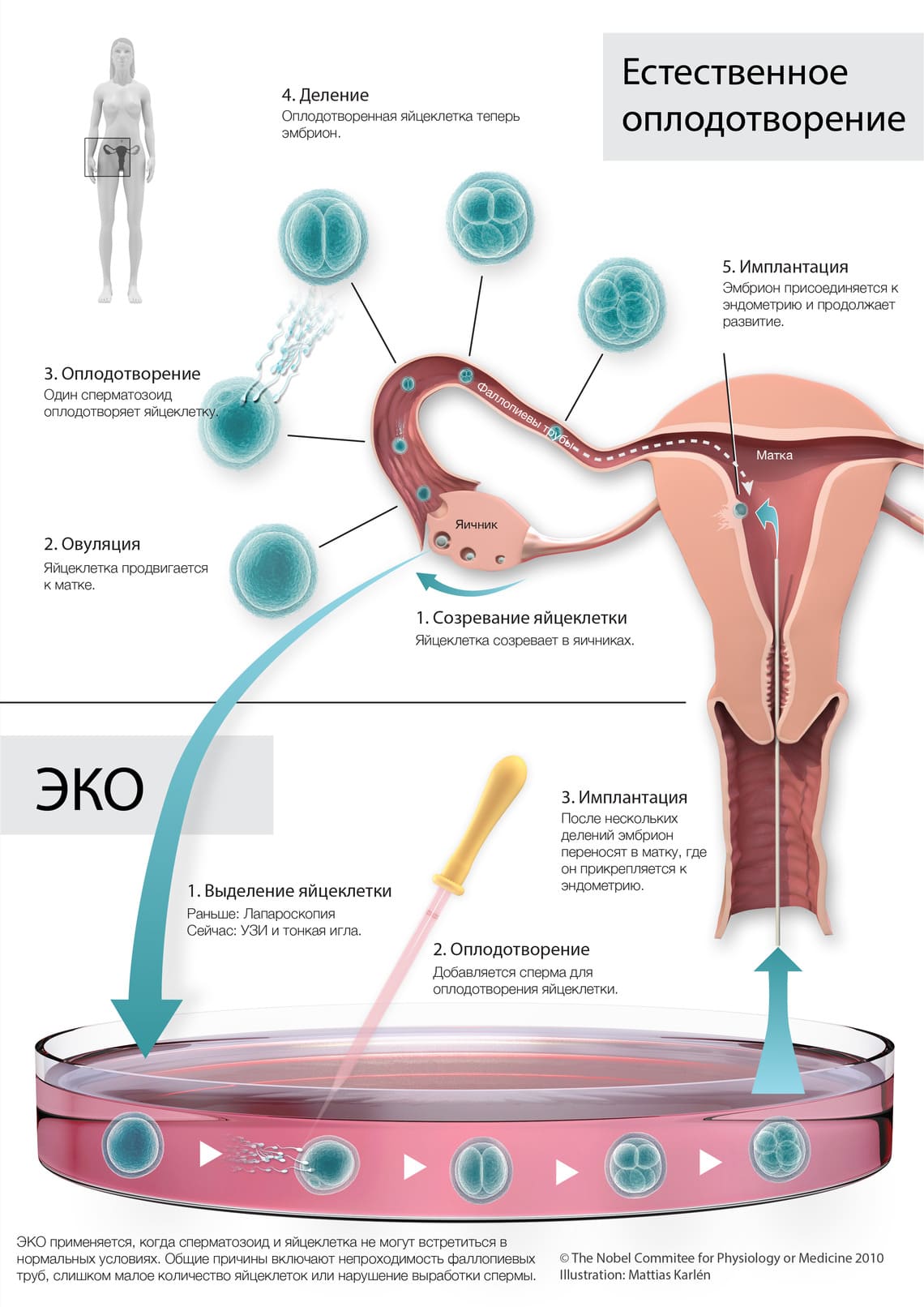
Рис. 2. Схемы естественного оплодотворения и ЭКО 2.
1. Индукция овуляции
Цикл ЭКО начинается со стимуляции яичников гонадотропинами — «суперовуляции» — с целью увеличения количества ооцитов, доступных для дальнейшего оплодотворения. Созревание ооцитов инициируется воздействием, подобным лютеинизирующему гормону (ЛГ), которое может обеспечиваться хорионическим гонадотропином человека (ХГЧ), агонистом гонадотропин-рилизинг гормона (ГнРГ), рекомбинантным ЛГ или кисспептином 6. Созревание яйцеклетки – критический процесс для успеха лечения ЭКО.
2. Получение ооцитов
Извлечение яйцеклеток осуществляется с помощью трансвагинальной пункции яичников под ультразвуковым контролем и внутривенной седации.
3. Оплодотворение in vitro
Осеменение или ИКСИ (интрацитоплазматическая инъекция сперматозоида) используется для оплодотворения ооцитов.
4. Перенос эмбрионов
Если оплодотворение прошло успешно, эмбрионам дают развиваться от 2 до 6 дней. Это помогает выбрать самый сильный эмбрион, который затем переносится обратно в матку женщины. Оплодотворенные эмбрионы обычно переносятся на стадии дробления (через 3 дня после оплодотворения) или на стадии бластоцисты (5 дней после оплодотворения).
Оставшиеся эмбрионы хорошего качества криоконсервируются для будущего использования, потому что помещение нескольких эмбрионов в матку увеличивает вероятность многоплодной беременности, что сопряжено с риском для здоровья 7, 3.
Немного статистики
Спустя 40 лет после рождения Луизы Браун, количество детей, рожденных в результате ЭКО, составляет уже более 8 миллионов 8.
Хотя эта практика варьируется в глобальном масштабе, в настоящее время она обеспечивает зачатие более 5% всех новорожденных в некоторых европейских странах, где ЭКО более доступно 9. В России в 2021 году было проведено более 80 тысяч процедур ЭКО, а до 2024 года предусмотрено проведение не менее 450 тысяч за счет бюджета 10.
Следует понимать, что наступление беременности зависит от многих факторов, таких как возраст, наследственность, состояние здоровья, причина и длительность бесплодия, образ жизни, качество эмбрионов, наличие неудачных попыток ЭКО 11. По миру вероятность успеха ЭКО составляет около 30% 12, 13. В России по статистике РАРЧ (Российская Ассоциация Репродукции Человека) на 2019 год для женщин до 34 лет она составила 22,8% 14.
ЭКО, как правило, очень безопасно, однако есть некоторые риски, о которых следует знать.
1. Синдром гиперстимуляции яичников (СГЯ)
СГЯ является осложнением при приеме гонадотропных препаратов: в яичниках развивается слишком много яйцеклеток большого размера. Синдром гиперстимуляции подразделяется на несколько стадий в зависимости от степени тяжести. Примерно у трети женщин бывает легкая форма СГЯ, которую обычно можно эффективно лечить в домашних условиях с помощью обезболивания. В очень редких случаях тяжелая форма СГЯ может быть опасной для жизни.
2. Многоплодная беременность или роды
При дальнейшем развитии беременности фактором риска является возникновение многоплодной беременности, которая может вызвать серьезные проблемы со здоровьем как у матери, так и у детей. Среди осложнений выделяют различные акушерские проблемы, недоношенность и рождение ребёнка с низким весом. Однако эти осложнения характерны не только для многоплодной, но и для одноплодной беременности 11.
3. Внематочная беременность
Все беременные женщины подвержены риску внематочной беременности, но женщины, проходящие ЭКО, подвергаются большему риску. Это связано с тем, что во время переноса эмбриона в матку он может попасть в маточную трубу 11, 15.
Эко животных
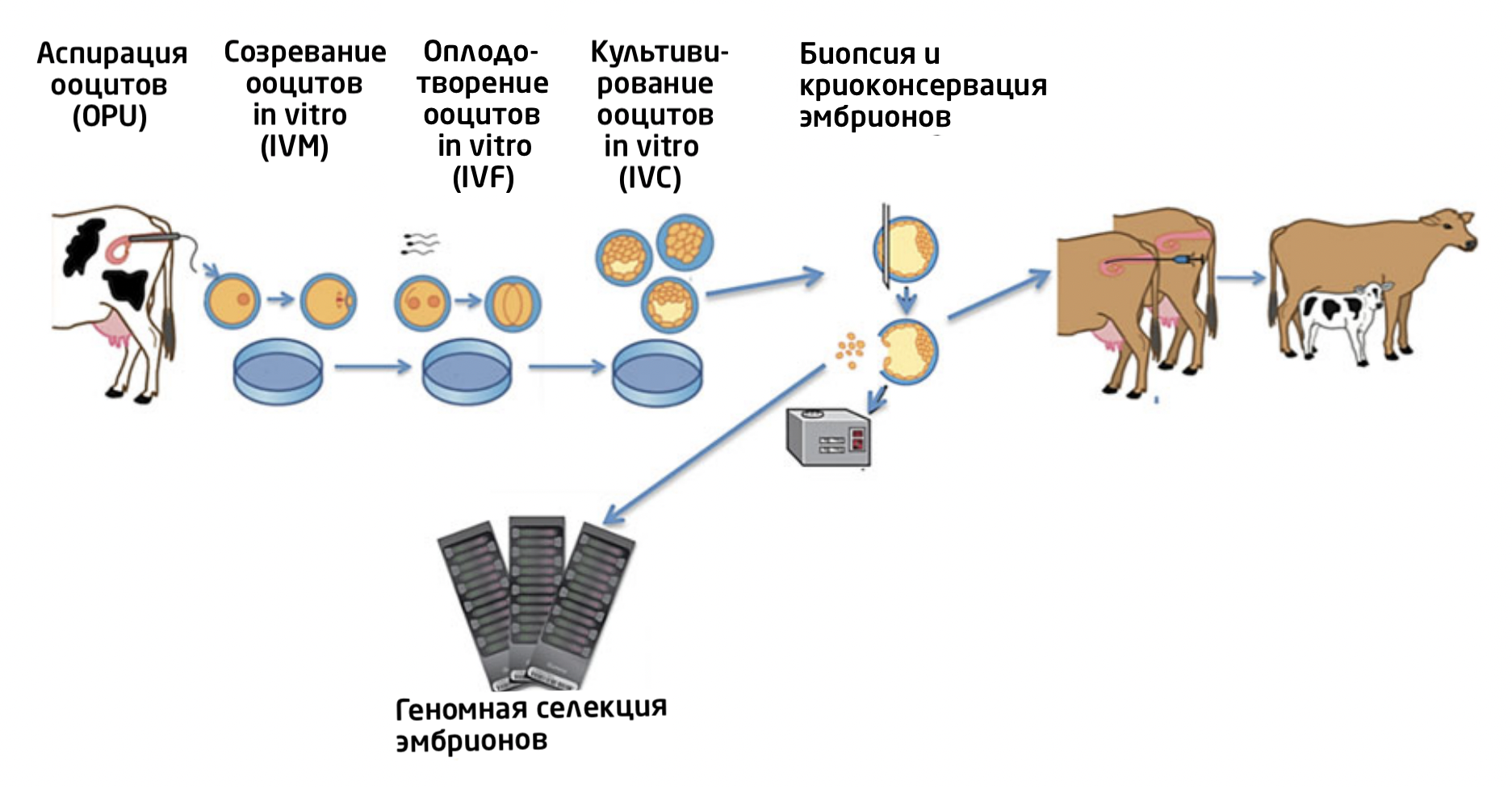
Хотя репродуктивные биологи начали эксперименты с ЭКО у кроликов еще в 50-х годах, только после рождения Лузины Браун возник интерес к другим крупным млекопитающим – особенно рогатому скоту. За последние 40 лет ЭКО животных превратилось из экспериментальной процедуры для лечения бесплодия в своеобразный геномный ускоритель для разных пород и видов по всему миру 16, 17, 5.
Рис. 3. Процесс ЭКО рогатого скота. Процедуры аспирации ооцитов (ovum pickup, OPU), созревания ооцитов in vitro (in vitro maturation, IVM), оплодотворения in vitro (in vitro fertilization, IVF) и культивированиe эмбрионов in vitro (in vitro culture, IVC) в совокупности называются производством эмбрионов in vitro (in vitro production, IVP) 18.
В отличие от людей, для большинства программ ЭКО животных не требуется процедур для суперовуляции. У обычных домашних животных обычно извлекают незрелые ооциты из яичников либо после обычной кастрации, при которой яичники удаляются, либо при процедурах забора яйцеклеток (OPU) у живых животных, либо после смерти животного (яичники животных в большинстве стран являются отходами мясной промышленности, поэтому их можно легко получить в больших количествах на скотобойнях). После созревания in vitro ооциты оплодотворяются, а затем культивируются до стадии развития эмбриона, подходящего для переноса. Также как и у людей, эмбрионы животных можно криоконсервировать.
Всё, в чем нуждается эмбрион для своего роста и развития, обеспечивает среда, в которой он культивируется. Поскольку в ЭКО животных практически весь процесс происходит in vitro, среды являются крайне важным компонентом на всех стадиях производства эмбрионов: сбор яйцеклеток, созревание ооцитов, подготовка спермы, оплодотворение, культивирование, перенос и транспортировка эмбрионов и т.д. 19, 20
В настоящее время рынок коммерческих сред, используемых для культивирования человеческих эмбрионов in vitro, велик — аналогичная тенденция наблюдается и в отношении ЭКО крупного рогатого скота. Коммерческие среды отличаются более стандартизированным составом, высоким контролем качества. Кроме того, их обычно тестируют на мышиных эмбрионах на предмет эффективности и безопасности 19, 20.
Сегодня индустрия ЭКО крупного рогатого скота стремительно развивается в масштабах, сравнимых с ЭКО человека, принося миллионы новорожденных в год. К основным преимуществам относятся увеличение числа потомков, сокращение интервала между поколениями, более широкий круг потенциальных доноров, экономия спермы и повышенные шансы на получение потомства с желаемой генетикой. Геномный анализ – одна из причин резкого увеличения ЭКО в животноводстве в последние годы, поскольку он стал инструментом отбора наиболее ценных особей уже на стадии эмбриона. Комбинация биопсии и криоконсервации эмбрионов привела к очень эффективной процедуре быстрого улучшения качества генома. Раньше этот процесс занимал несколько лет.
ЭКО также позволяет сохранять исчезающие виды и получать потомство от непродуктивных животных. Кроме того, во многих случаях животных можно использовать в качестве моделей для людей в отношении окончательного созревания ооцитов, оплодотворения и раннего развития эмбрионов in vitro 18, 21.
Сегодня лидером мирового рынка ЭКО животных является компания IVF Bioscience. Это дочерняя фирма Research Instruments Ltd, крупнейшего мирового игрока, специализирующегося на поставках оборудования для in vitro оплодотворении человека.
В портфолио компании IVF Bioscience представлены среды для ЭКО, ИКСИ, переноса полученных методом in vitro эмбрионов, а также клонирования животных. Все среды производятся по стандартам ЭКО человека.
Проблемы и будущее ЭКО
Первоначально ЭКО разрабатывали для лечения бесплодия, однако сегодня клинические показания расширились и включают, к примеру, сохранение фертильности. Вполне вероятно, что в ближайшем будущем во многих частях мира с помощью ЭКО будет зачато до 10% всех детей. Однако стремительное развитие ЭКО в последние годы еще не означает, что технология полностью отработана. Предстоит решить ряд проблем, и многие процедуры все еще нуждаются в оптимизации 9.
Процесс ЭКО сложный, длительный, чувствительный ко времени и интенсивный. Основными причинами преждевременного отказа пациентов от ЭКО являются финансовые, физические и психологические трудности. Использование ЭКО может значительно вырасти в ближайшие десятилетия, если процесс будет упрощаться, например, за счет сокращения количества инъекций или более простых процедур мониторинга. Внедрение автоматизированных систем также даст множество преимуществ, таких как стандартизация рабочих процессов, снижение количества ошибок, контаминации и затрат.
Важно, чтобы внедрение инновационных технологий в клиническую практику основывалось на науке и поддерживалось клиническими испытаниями. Преждевременная коммерциализация дорогостоящих и непроверенных «дополнений» к ЭКО была постоянной проблемой в этой области 22.
Конечно, ЭКО не скоро исчезнет и из набора инструментов для селекции животных. Новые подходы, часто разрабатываемые на людях, могут стать доступными для крупного рогатого скота и улучшить показатели беременности 16. С появлением новых инструментов для редактирования генома и даже эпигенома CRISPR-Cas9 и TALEN возрос интерес к генетическим модификациям животных, предназначенным как для производства, так и для исследований 17.
Все еще существуют недостатки, которые ограничивают более широкое внедрение ЭКО у животных. Все еще существуют недостатки, которые ограничивают более широкое внедрение ЭКО у животных. Особое внимание уделяется разработке и улучшению качества сред – по мере их усложнения возрастает вероятность лабораторных ошибок, которые снижают, например, качество ооцитов после созревания, криотолерантность эмбрионов и, в результате, частоту наступления беременности и эффективность ЭКО 18, 19. Поэтому неудивительно, что качество их состава было и остается предметом многочисленных исследований, направленных на оптимизацию условий культивирования и повышение показателей успеха ЭКО животных. Важно потенциально производить потомство, ничем не отличающееся от зачатого in vivo 19.
Интересно, что искусственный интеллект обещает революционные изменения в области ЭКО благодаря способности прогнозировать клинические исходы. Например, ИИ может помочь в выборе наилучшей комбинации ооцитов и сперматозоидов, прогнозировании качества эмбрионов и даже разработать оптимальную схему лечения для конкретного пациента 23.
Технология ЭКО навсегда изменила репродуктивную медицину и за короткий срок стала новой нормой. Нам еще предстоит пройти долгий путь, но непрекращающиеся исследования в эмбриологии человека и животных постепенно ведут к оптимизации текущих протоколов ЭКО и разработке новых подходов для повышения как безопасности, так и эффективности метода.
Литература
1. Infertility. World Health Organization.
2. Press release: The Nobel Prize in Physiology or Medicine 2010. The Nobel Prize, 2010.
3. Choe J. et al. In Vitro Fertilization. StatPearls, 2022.
4. Johnson M.H. A short history of in vitro fertilization (IVF). The International Journal of Developmental Biology, 2019.
5. Дороничева Д.А., Стулева Н.С. Основные вехи истории экстракорпорального оплодотворения. Акушерство, Гинекология и Репродукция, 2020.
6. Abbara A. et al. Novel Concepts for Inducing Final Oocyte Maturation in In Vitro Fertilization Treatment. Endocrine Reviews, 2018.
7. Handbook of In Vitro Fertilization. 2017.
8. European Society of Human Reproduction and Embryology. More than 8 million babies born from IVF since the world's first in 1978. Science Daily, 2018.
9. Kushnir V.A. et al. The Future of IVF: The New Normal in Human Reproduction. Reproductive Sciences, 2022.
10. Манукиян Е. Стало известно число ЭКО, выполненных в России в 2021 году. Российская Газета, 2022.
11. Zollner U., Dietl J. Perinatal risks after IVF and ICSI. Journal of Perinatal Medicine, 2013.
12. IVF success rates. IVF Australia.
13. ART Success Rates. Centers for Disease Control and Prevention.
14. Регистр ВРТ. Российская Ассоциация Репродукции Человека, 2019.
15. In vitro fertilisation (IVF). Human Fertilisation and Embryology Autority.
16. Sirard M. 40 years of bovine IVF in the new genomic selection context. Reproduction, 2018.
17. Sjunnesson Y. In vitro fertilisation in domestic mammals - a brief overview. Upsala Journal of Medical Sciences, 2020.
18. Ferré L.B. et al. Review: Recent advances in bovine in vitro embryo production: reproductive biotechnology history and methods. Animal, 2019.
19. Chronopoulou E., Harper J.C. IVF culture media: past, present and future. Human Reproduction Update, 2015.
20. Prochowska S. et al. The use of human and bovine commercial media for oocyte maturation and embryo development in the domestic cat (Felis catus). Reproduction in Domestic Animals, 2019.
21. Hasler J.F. Forty years of embryo transfer in cattle: a review focusing on the journal Theriogenology, the growth of the industry in North America, and personal reminisces. Theriogenology, 2014.
22. Gleicher N. et al. Worldwide decline of IVF birth rates and its probable causes. Human Reproduction Open, 2019.
23. Chow D.J.X. et al. Does artificial intelligence have a role in the IVF clinic? Reproduction Fertility, 2021.




.jpg)